
 学术中心Academic Centers
学术中心Academic Centers
联系我们
SSTR2标记物在实体瘤诊疗中的应用
浏览次数:4870 发布时间:2021-11-01
生长抑素作为一种由体内多种组织产生分泌并且广泛存在的激素,其主要作用是抑制垂体生长激素和胃泌素的分泌。天然生长抑素半衰期较短(约2~3分钟),限制了其在临床上的应用,人工合成的生长抑素类似物(SSTA)选择性强、半衰期长,主要有奥曲肽、兰瑞肽等。生长抑素受体(somatostatin receptor,SSTR)[1]作为G 蛋白偶连信号转导通路的受体,可阻止原癌基因的激活,抑制细胞的增殖,也可以通过MAPK 途径使酪氨酸激酶失活,从而阻止细胞的增殖[2]。
SSTRs有5种不同的亚型(SSTR1~5),在正常组织和神经内分泌肿瘤中广泛表达,并具有亚型选择性和组织特异性。例如,在功能性垂体腺瘤组织中,生长激素分泌腺瘤主要表达SSTR2和SSTR5,在非功能性垂体肿瘤和胃肠胰神经内分泌肿瘤(胃泌素瘤、胰高血糖素瘤和胰 岛素瘤)中,5种生长抑素受体都有表达,特别是SSTR2 和SSTR5表达很普遍[5]。近年来,发现SSTRs在多种常见的癌症中表达,包括肝癌、肺癌、胰腺癌、前列腺癌和乳腺癌等实体瘤中[6]。根据对序列同源性以及配体结合能力的分析,5种亚型的受体可分为两类:一类是SSTR2、SSTR3以及SSTR5,另一类是SSTR1和SSTR4。前者对于合成的生长抑素类似物(SSTA)的亲和力明显高于后者。因此,目前临床检测优先检测SSTR2和SSTR5。
一、肿瘤组织SSTR免疫组化检测意义
神经内分泌肿瘤(NENs)近年来全球范围内发病逐年增加,目前发病率约为4~5/10万,除原发于胸腺和肺的神经内分泌肿瘤外,其余几乎均来源于消化系统,包括食管、胃肠道和胰腺等。对于转移性分化好的神经内分泌瘤,目前可选择的药物治疗主要包括生长抑素类似物、靶向药物和化疗药物,主要以控制肿瘤进展为主,客观有效率相对偏低,而且接受上述药物治疗进展后疾病很难控制。肽受体介导的放射性核素治疗(PRRT)是利用放射性核素标记的生长抑素类似物与体内肿瘤的生长抑素受体结合发挥抗肿瘤治疗作用,而90%的神经内分泌肿瘤存在生长抑素受体表达,PRRT是治疗分化好的生长抑素受体表达阳性的神经内分泌肿瘤的一项重要手段,在欧美已开展多年。PRRT已成为ENETs和NCCN神经内分泌肿瘤指南共识里重要的推荐治疗之一,2018年美国FDA正式批准Lutetium-177(177Lu)标记的生长抑素类似物用于胃肠胰神经内分泌肿瘤的治疗。PRRT治疗的依据是对组织SSTR是否表达及量的多少的检测结果。
消化系统的神经内分泌肿瘤的新分类明确了神经内分泌瘤(NET)G1/G2/G3和神经内分泌癌(NEC),在NET G3和NEC之间(Ki67增值指数在20~50%),即使可以依据形态进行诊断,但是还是有一些病例特别是活检的病例难于诊断,除了IHC检测p53、Rb外,我们还可以增加SSTR2的检测,SSTR2在NET G3中呈强表达,在NEC中表达弱甚至不表达。
二、SSTR的判读方法
1、 Volante Score[7]标准
依据:膜染色是否完整,肿瘤细胞占比是否超过50%。
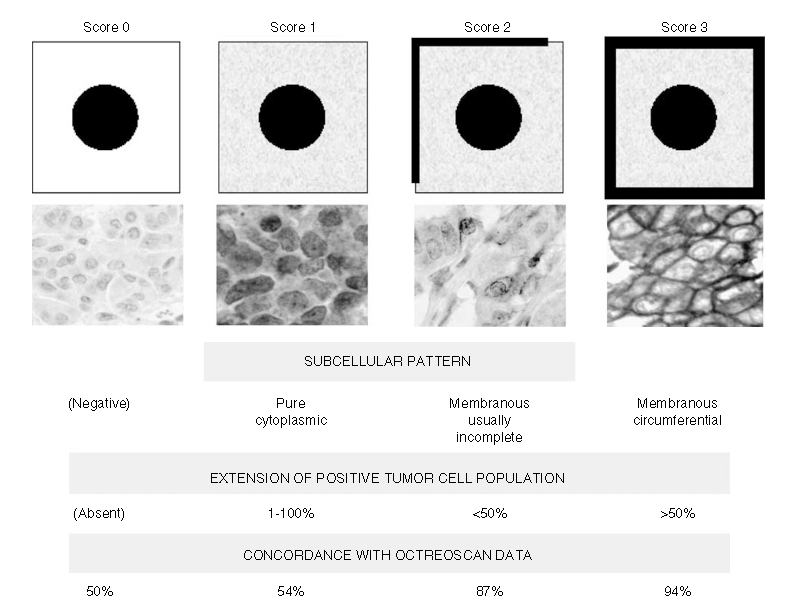
2、 HER2/Neu[8]标准
依据:膜或浆是否着色,肿瘤细胞占比是否超过10%。
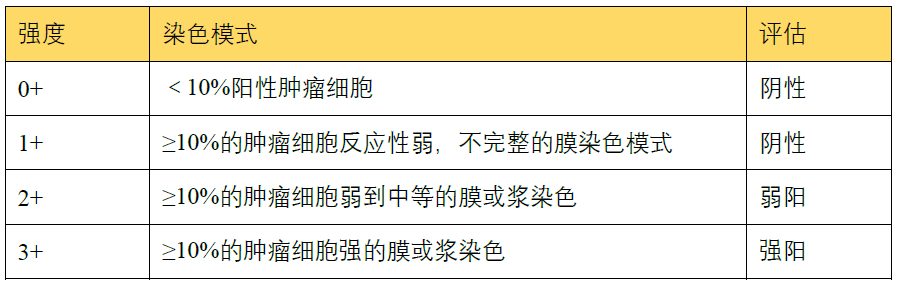
3、Remmele und Stegner(IRS)标准
依据:细胞染色强度,肿瘤细胞占比(10%,50%,80%)。
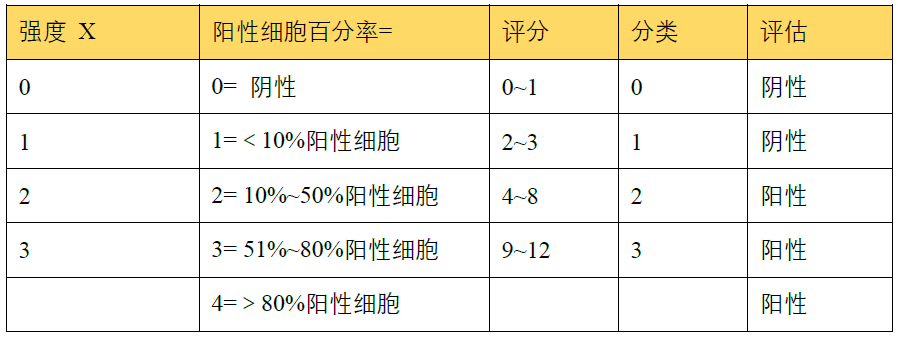
4、H-Score标准
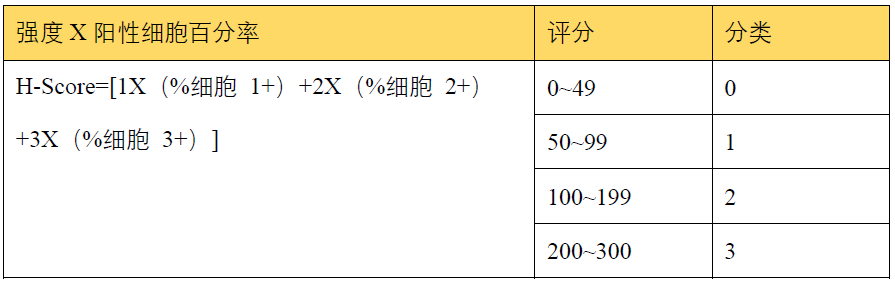
2家国外研究机构(分别来自意大利和日本)就SSTR表达情况及与合成的生长抑素类似物(SSTA)的临床反应性做了综合性的评估[9]。评估样本包括38例NET患者的52个组织;IHC染色平台涉及1种自动化和2种手动;评估人员包括2名经验丰富的病理学家和1名医学生;染色结果评估系统包括:Volante、Her2和H评分;采用分别对病理切片进行了独立的评估方式。结果显示各种染色方法所得的分数彼此高度相关(r>0.85,P<0.0001),其中Volante和Her2评分高度一致(r≥0.95,P≤0.0001);Her2评分评估的SSTR2a[Lc1] 表达与生长抑素类似物的临床效果显著相关,可作为神经内分泌肿瘤中SSTR2A和SSTR5表达的标准评估方法。
三、产品信息

参考文献
[1] Xin-Xiu X U, Zhang L H, Xie X. Somatostatin receptor type 2 contributes to the self-renewal of murine embryonic stem cells[J]. 中国药理学报:英文版,2014,35(008):1023-1030.
[2] 陈书凯,钟文萍,周天鸿,等. 生长抑素受体在人神经内分泌癌组织中的表达及受体激活对细胞生长的抑制[J]. 中国生物化学与分子生物学报,2018,034(003):310-317.
[3] Schmid H A, Lambertini C, Van Vugt H H, et al. Monoclonal antibodies against the human somatostatin receptor subtypes 1-5: development and immunohistochemical application in neuroendocrine tumors.[J]. Neuroendocrinology,2012,95(3):232-247.
[4] E K V A, A M X, A T S M, et al. Differential somatostatin receptor (SSTR) 1–5 expression and downstream effectors in histologic subtypes of growth hormone pituitary tumors - ScienceDirect[J]. Molecular and Cellular Endocrinology,2015,417:73-83.
[5] Song K B, Kim S C, Kim J H, et al. Prognostic Value of Somatostatin Receptor Subtypes in Pancreatic Neuroendocrine Tumors[J]. Pancreas,2015,45(2):187.
[6] Gupta D, Gupta V, Marwah N, et al. Correlation of Hormone Receptor Expression with Histologic Parameters in Benign and Malignant Breast Tumors[J]. Iranian Journal of Pathology,2015,10(1):23.
[7] Volante M, Brizzi M P, Faggiano A, et al. Somatostatin receptor type 2A immunohistochemistry in neuroendocrine tumors: a proposal of scoring system correlated with somatostatin receptor scintigraphy[J]. Modern pathology,2007,20(11):1172-1182.
[8] Specht, Elisa, Kaemmerer, et al. Comparison of immunoreactive score, HER2/neu score and H score for the immunohistochemical evaluation of somatostatin receptors in bronchopulmonary neuroendocrine neoplasms[J].
[9] Kasajima A, Papotti M, Ito W, et al. High interlaboratory and interobserver agreement of somatostatin receptor immunohistochemical determination and correlation with response to somatostatin analogs[J]. Human Pathology,2018,72:144-152.


